研究テーマ
ミトコンドリアと疾患・老化:細胞内代謝プラントとしての役割を知り、ミトコンドリアを標的にした創薬に挑む
近年のミトコンドリア研究のめざましい進展により、ミトコンドリアは「エネルギー産生を担う均質な豆状オルガネラ」という古典的概念から、「シグナルを検知・処理し、発信する高次機能を制御するオルガネラ」という新たな姿に変貌しました。このような多彩な機能を持つミトコンドリアの機能異常が、ミトコンドリア病のみならず老化や代謝異常を基盤とするさまざまな疾患に関連することは必然とも言えます。当研究室では世界に先駆けてミトコンドリア外膜を4回貫通するユニークな膜型E3ユビキチンリガーゼMITOL(マイトル)を発見することに成功しました。これまでにMITOLがミトコンドリアの形態制御や品質管理を担っていること、ミトコンドリアと小胞体との接着構造の形成を制御していることなどを明らかにしてきました。
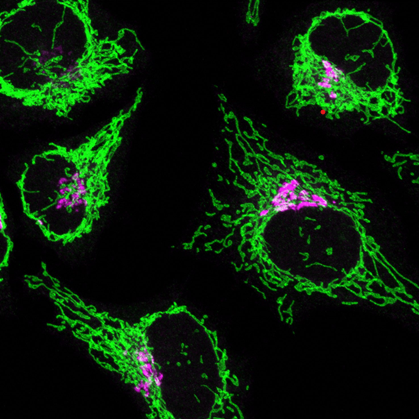
今後、私たちはMITOLによるミトコンドリア膜上のユビキチン化を介したシグナル伝達応答の解析を通して、ミトコンドリア動態の制御機構、オルガネラコンタクト(細胞小器官の相互作用)形成の分子機構、新たなシグナル伝達制御機構の同定と生理意義の解明を目指します。さらに、病態との関連およびミトコンドリアを標的にした新たな創薬開発に挑みます。
1. ミトコンドリア動態の制御機構
ミトコンドリア動態(ダイナミクス)は、ミトコンドリアの融合・分裂による形態制御、ミトコンドリアの微小管上での移動、小胞体などの他のオルガネラとの相互作用を包括する機能的概念です。ミトコンドリア動態の破綻は神経変性疾患や心不全などさまざまな疾患を引き起こすことが示唆されています。私たちはこれまでMITOLがミトコンドリア分裂因子Drp1をユビキチン化して分解を促進すること、反対にミトコンドリア融合因子Mfn2を活性化することによってミトコンドリア動態を調節していることを報告してきました(Yonashiro et al., EMBO J. 2006, Yonashiro et al., Proc. Natl. Acad. Sci. USA 2012, Sugiura et al., Mol. Cell 2013)。このようにMITOLはミトコンドリア動態を制御する中心的な酵素ですが、未だ詳細な分子機構は不明です。最近私たちは、心筋特異的MITOL欠損マウスを解析したところミトコンドリアの形態異常によって重度の心不全を発症する可能性を示しました。今後、MITOLによるミトコンドリア動態の制御機構とその生理的意義について、細胞及び個体レベルの解析を通して、ミトコンドリア動態の破綻と病態との関連を解明し、新たな創薬の標的を提示したいと考えています。
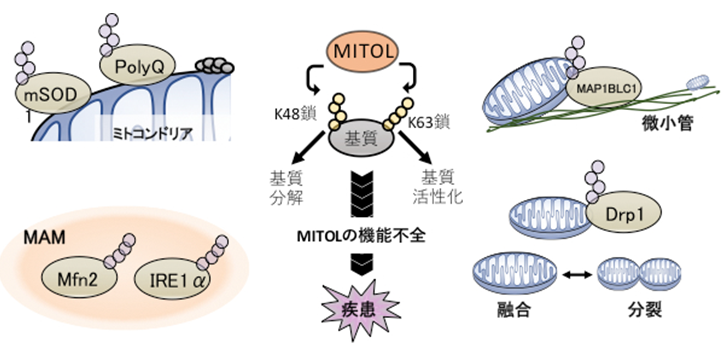
2. オルガネラコンタクトの分子機構と生理機能
オルガネラコンタクトの代表例であるミトコンドリアと小胞体の接着構造は、Mitochondria-associated ER membrane(MAM)とも呼ばれ、効率的な脂質代謝物質の輸送やCa2+の受け渡しを可能にしています。さらに近年、MAMがミトコンドリアの分裂部位の決定に関与すること、オートファゴソームの隔離膜の形成やインフラマソームの形成に関与すること、自然免疫応答のシグナル伝達の足場として機能することなど多彩な役割が報告されており、MAMの生理的重要性がますます注目を集めています。Mfn2はミトコンドリア外膜と小胞体膜の両方に局在し、お互いに重合することによって小胞体とミトコンドリアを架橋する繋留因子として知られていましたが、Mfn2の活性調節機構は不明でした。私たちはMITOLがMfn2をユビキチン化することによってMfn2の重合を促進してMAMの形成を誘導することを世界で初めて明らかにしました(Mol. Cell 2013)。その後、MITOLが生体内においてもMAM形成に必須であることを証明しました(Nagashima et al., Life Sci. Alliance 2019)。さらに、MAMにおいてMITOLが小胞体ストレスセンサーであるIRE1の過剰活性化を抑制して細胞死を回避する新たなシグナル伝達応答機構を明らかにしました(Takeda et al., EMBO J. 2019)。今後、MITOLの機能解析を通してオルガネラコンタクトの基本原理の解明を目指します。
3. ミトコンドリアと疾患
パーキンソン病は中脳黒質のドーパミン作動性神経が脱落することにより振戦・固縮などの錐体外路症状を呈する神経変性疾患の一つで、ミトコンドリアの機能異常が主な原因であると考えられています。家族性パーキンソン病の原因遺伝子の一つであるParkinは膜電位の低下した劣化ミトコンドリアを特異的に認識して排除するマイトファジーの実行因子として知られています。私たちはMITOLがParkinを制御することによりパーキンソン病の病態に密接に関与することを見出しており、MITOLを活性化する薬剤はパーキンソン病の特効薬になるのではないかと期待しています。さらにMITOLはアルツハイマー病やALSなどの神経変性疾患、心不全、皮膚老化など様々な老化疾患との関連が示唆されています(Yonashiro et al., Mol. Biol. Cell 2009)。今後、臓器特異的MITOL欠損マウスの解析を通して、ミトコンドリア機能不全による疾患の病態を解明し、MITOLを標的にした治療法開発に挑戦したいと考えています。
4. ミトコンドリアを標的にした抗老化薬の開発
皮膚組織特異的MITOL欠損マウスは、早期から顕著な白髪・脱毛が認められ、病理組織解析においても皮膚の老化所見が観察されました。また、正常のマウス皮膚組織においてもMITOLの発現が老化と共に有意に減少することより、MITOLの発現低下は活性酸素種の産生を誘導し老化を引き起こす可能性が示されました。そこで、MITOLの発現を誘導する薬剤は老化を抑制できるのではないかと考え、製薬会社との共同研究でMITOLの発現を誘導する薬剤を同定しました。これらの薬剤をマウスに服用させた結果、皮膚老化を顕著に抑制する結果が得られました。今後、さまざまな化合物(天然物抽出液など)ライブラリーからMITOLの発現を促進する薬剤をスクリーニングし、ミトコンドリアを標的としたサプリメント、化粧品、医薬品を含めた抗老化薬の開発を目指します。
活動実績
主な原著論文
Shiiba, I., Ishikawa, Y., Oshio, H., Ito, N., Yamaguchi, F., Nagashima, S., Ando, H., Umezawa, K., Miura, Y., Araiso, Y., Nakamura, K., Hirabayashi, Y., Inatome, R., and Yanagi, S.
MFN2-STIM1-Mediated Mitochondria-Melanosome Contact: A Key to Melanosome Maturation.
Nat. Commun. in press PMID: 41862479
Sato, M., Tanabu, D., Torigoe, D., Kadomatsu, T., Taniwaka, K., Ogata, Y., Shiiba, I., Suzuki, Y., Ito, N., Inatome, R., Tokuyama, T., Takeiwa, T., Inoue, S., Kanai, E., Hamano, T., Hirata, H., Kanamitsu, K., Kusuhara, H., Yokosuka, A., Mimaki, Y., Abe, H., Oike, Y., and Yanagi, S.
Mitorubin, berberrubine-based compounds that improve mitochondrial function, exhibit cardioprotective effects against age-related cardiac dysfunction.
npj aging. in press PMID: 41792161
Oshio, H., Shiiba, I., Takeda, A., Matsumoto, S., Ishikawa, Y., Nagashima, S., Inatome, R., and Yanagi, S.
Role of lipoylation in mitochondrial supercomplex formation during C2C12 cell differentiation.
J. Biochem. mvag014 (2026) PMID: 41717828
Ishikawa, Y., Shiiba, I., Kozakura, E., Yabu, H., Hirose, S., Oshio, H., Yamada, K.I., Okamatsu-Ogura, Y., Inatome, R., and Yanagi, S.
Palmitic acid induces UCP1-independent mitochondrial depolarization specifically in brown adipose tissue.
J. Biol. Chem. 302(3), 111177 (2026) PMID: 41570989
Shiiba, I., Ito, N., Oshio, H., Ishikawa, Y., Nagao, T., Shimura, H., Oh, K.W., Takasaki, E., Yamaguchi, F., Konagaya, R., Kadowaki, H., Nishitoh, H., Tanzawa, T., Nagashima, S., Sugiura, A., Fujikawa, Y., Umezawa, K., Tamura, Y., Lee, B.I., Hirabayashi, Y., Okazaki, Y., Sawa, T., Inatome, R., and Yanagi, S.
ER-mitochondria contacts mediate lipid radical transfer via RMDN3/PTPIP51 phosphorylation to reduce mitochondrial oxidative stress.
Nat. Commun. 16(1), 1508 (2025) PMID: 39929810
Tokuyama, T., Uosaki, H., Sugiura, A., Nishitai, G., Takeda, K., Nagashima, S., Shiiba, I., Ito, N., Amo, T., Mohri, S., Nishimura, A., Nishida, M., Konno, A., Hirai, H., Ishido, S., Yoshizawa, T., Shindo, T., Takada, S., Kinugawa, S., Inatome, R., and Yanagi, S.
Protective roles of MITOL against myocardial senescence and ischemic injury partly via Drp1 regulation.
iScience 25(7), 04582 (2022) PMID: 35789860
Ito, N., Takahashi, T., Shiiba, I., Nagashima, S., Inatome, R., and Yanagi, S.
MITOL regulates phosphatidic acid-binding activity of RMDN3/PTPIP51.
J. Biochem. 171(5), 529-541 (2021) PMID: 34964862
Nagashima, S., Ito, N., Kobayashi, R., Shiiba, I., Shimura, H., Fukuda, T., Hagihara, H., Miyakawa, T., Inatome, R., and Yanagi, S.
Forebrain-specific deficiency of the GTPase CRAG/Centaurin-γ3 leads to immature dentate gyri and hyperactivity in mice.
J. Biol. Chem. 296, 100620 (2021) PMID: 33811862
Mitsubori, M., Takeda, K., Nagashima, S., Ishido, S., Matsuoka, M., Inatome, R., and Yanagi, S.
Identification of highest neurotoxic amyloid-β plaque type showing reduced contact with astrocytes.
Biochem. Biophys. Res. Commun. 549, 67-74 (2021) PMID: 33667711
Takeda, K., Uda, A., Mitsubori, M., Nagashima, S., Iwasaki, H., Ito, N., Shiiba, I., Ishido, S., Matsuoka, M., Inatome, R., and Yanagi, S.
Mitochondrial ubiquitin ligase alleviates Alzheimer's disease pathology via blocking the toxic amyloid-β oligomer generation.
Commun. Biol. 4, 192 (2021) PMID: 33580194
Shiiba, I., Takeda, K., Nagashima, S., Ito, N., Tokuyama, T., Yamashita, S.I., Kanki, T., Komatsu, T., Urano, Y., Fujikawa, Y., Inatome, R., and Yanagi, S.
MITOL promotes cell survival by degrading Parkin during mitophagy.
EMBO Rep. e49097 (2021) PMID: 33565245
Tokuyama, T., Hirai, A., Shiiba, I., Ito, N., Matsuno, K., Takeda, K., Saito, K., Mii, K., Matsushita, N., Fukuda, T., Inatome, R., and Yanagi, S.
Mitochondrial Dynamics Regulation in Skin Fibroblasts from Mitochondrial Disease Patients.
Biomolecules 10(3), E450 (2020) PMID: 32183225
Matsuno, K., Nagashima, S., Shiiba, I., Taniwaka, K., Takeda, K., Tokuyama, T., Ito, N., Matsushita, N., Fukuda, T., Ishido, S., Inatome, R., and Yanagi, S.
MITOL dysfunction causes dwarfism with anterior pituitary hypoplasia.
J. Biochem. 168(3), 305-312 (2020) PMID: 32302394
Takeda, K., Nagashima, S., Shiiba, I., Uda, A., Tokuyama, T., Ito, N., Fukuda, T., Matsushita, N., Ishido, S., Iwawaki, T., Uehara, T., Inatome, R., and Yanagi, S.
MITOL prevents ER stress-induced apoptosis by IRE1α ubiquitylation at ER-mitochondria contact sites.
EMBO J. e100999 (2019) PMID: 31196886
Nagashima, S., Takeda, K., Shiiba, I., Higashi, M., Fukuda, T., Tokuyama, T., Matsushita, N., Nagano, S., Araki, T., Kaneko, M., Shioi, G., Inatome, R., and Yanagi, S.
Critical role of CRAG in ELK1-dependent SRF activation at PML bodies.
Sci. Rep. 9(1), 20107 (2019) PMID: 31882856
Nagashima, S., Takeda, K., Ohno, N., Ishido, S., Aoki, M., Saitoh, Y., Takada, T., Tokuyama, T., Sugiura, A., Fukuda, T., Matsushita, N., Inatome, R., and Yanagi, S.
MITOL deletion in the brain impairs mitochondrial structure and ER tethering leading to oxidative stress.
Life Sci. Alliance 2(4), e201900308 (2019) PMID: 31416892
Fukuda, T., Nagashima, S., Inatome, R., and Yanagi, S.
CAMDI interacts with KIBRA and regulates AMPAR expression.
PLoS ONE 14(11), e0224967 (2019) PMID: 31730661
Matsushita, N., Suzuki, M., Ikebe, E., Nagashima, S., Inatome, R., Asano, K., Tanaka, M., Matsushita, M., Kondo, E., Iha, H., and Yanagi, S.
Regulation of B cell differentiation by the ubiquitin-binding protein TAX1BP1.
Sci. Rep. 6, 31266 (2016) PMID: 27515252
Fukuda, T., Nagashima, S., Abe, T., Kiyonari, H., Inatome, R., and Yanagi, S.
Rescue of CAMDI deletion-induced delayed radial migration and psychiatric behaviors by HDAC6 inhibitor.
EMBO Rep. 17(12), 1785-1798 (2016) PMID: 27737934
Sugiura, A., Nagashima, S., Tokuyama, T., Amo, T., Matsuki, Y., Ishido, S., Kudo, Y., McBride, H.M., Fukuda, T., Matsushita, N., Inatome, R., and Yanagi, S.
MITOL regulates endoplasmic reticulum-mitochondria contacts via mitofusin2.
Mol. Cell 51(1), 20-34 (2013) PMID: 23727017
Yonashiro, R., Kimijima, Y., Shimura, T., Kawaguchi, K., Fukuda, T., Inatome, R., and Yanagi, S.
MITOL blocks S-nitrosylated MAP1B-light chain 1-mediated mitochondrial dysfunction and neuronal cell death.
Proc. Natl. Acad. Sci. U.S.A. 109(7), 2382-2387 (2012) PMID: 22308378
Sugiura, A., Yonashiro, R., Fukuda, T., Matsushita, N., Nagashima, S., Inatome, R., and Yanagi, S.
MITOL controls cell toxicity of polyglutamine-expanded protein.
Mitochondrion 11(1), 139-146 (2011) PMID: 20851218
Nagashima, S., Fukuda, T., Kubota, Y., Sugiura, A., Nakao, M., Inatome, R., and Yanagi, S.
CRAG protects neuronal cells against cytotoxicity of expanded polyglutamine protein.
J. Biol. Chem. 286(39), 33879-33889 (2011) PMID: 21832068
Matsushita, N., Yonashiro, R., Ogata, Y., Sugiura, A., Nagashima, S., Fukuda, T., Inatome, R., and Yanagi, S.
Distinct regulation of mitochondrial localization and stability of two human Sirt5 isoforms.
Genes Cells 16(2), 190-202 (2011) PMID: 21143562
Matsushita, N., Endo, Y., Sato, K., Kurumizaka, H., Yamashita, T., Takata, M., and Yanagi, S.
Direct inhibition of TNF-α promoter activity by FANCD2.
PLoS ONE 6(8), e23324 (2011) PMID: 21912593
Fukuda, T., Sugita, S., Inatome, R., and Yanagi, S.
CAMDI is required for radial migration.
J. Biol. Chem. 285(52), 40554-40561 (2010) PMID: 20956536
Yonashiro, R., Sugiura, A., Miyachi, M., Fukuda, T., Matsushita, N., Inatome, R., Ogata, Y., Suzuki, T., Dohmae, N., and Yanagi, S.
MITOL ubiquitinates mutant SOD1 and attenuates ROS generation.
Mol. Biol. Cell 20(21), 4254-4530 (2009) PMID: 19741096
Yonashiro, R., Ishido, S., Kyo, S., Fukuda, T., Goto, E., Matsuki, Y., Ohmura-Hoshino, M., Sada, K., Hotta, H., Yamamura, H., Inatome, R., and Yanagi, S.
A novel mitochondrial ubiquitin ligase plays a critical role in mitochondrial dynamics.
EMBO J. 25(15), 3618-3626 (2006) PMID: 16874301
Qin, Q., Inatome, R., Hotta, A., Kojima, M., Yamamura, H., Hirai, H., Yoshizawa, T., Tanaka, H., Fukami, K., and Yanagi, S.
CRAG mediates nuclear body formation and degradation of polyglutamine protein.
J. Cell Biol. 172(4), 497-504 (2006) PMID: 16461359
Hotta, A., Inatome, R., Yuasa-Kawada, J., Qin, Q., Yamamura, H., and Yanagi, S.
CRAM is critical for filopodia and growth cone development.
Mol. Biol. Cell 16(1), 32-39 (2005) PMID: 15509652
Takahashi, S., Inatome, R., Yamamura, H., and Yanagi, S.
A novel mitochondrial septin interacting with CRMP/CRAM.
Genes Cells 8(2), 81-93 (2003) PMID: 12581152
Takahashi, S., Inatome, R., Hotta, A., Qin, Q., Hackenmiller, R., Simon, M.C., Yamamura, H., and Yanagi, S.
Role for Fes/Fps tyrosine kinase in microtubule nucleation.
J. Biol. Chem. 278(49), 49129-49133 (2003) PMID: 14551201
Mitsui, N., Inatome, R., Takahashi, S., Goshima, Y., Yamamura, H., and Yanagi, S.
Fes/Fps kinase in semaphorin3A signaling.
EMBO J. 21(13), 3296-3306 (2002) PMID: 12093729
Yanagi, S., Inatome, R., Ding, J., Kitaguchi, H., Tybulewicz, V.L., and Yamamura, H.
Syk expression and defects in Syk-deficient mice.
Blood 98(9), 2869-2871 (2001) PMID: 11675365
Inatome, R., Tsujimura, T., Hitomi, T., Mitsui, N., Hermann, P., Kuroda, S., Yamamura, H., and Yanagi, S.
Identification of CRAM protein in developing brain.
J. Biol. Chem. 275(35), 27291-27302 (2000) PMID: 10851247
Yanagi, S., Sugawara, H., Kurosaki, M., Sabe, H., Yamamura, H., and Kurosaki, T.
CD45 modulates Lyn phosphorylation in B cells.
J. Biol. Chem. 271(48), 30487-30492 (1996) PMID: 8940015
Yanagi, S., Sada, K., Tohyama, Y., Tsubokawa, M., Nagai, K., Yonezawa, K., and Yamamura, H.
p72syk activation and PI3K association in platelets.
Eur. J. Biochem. 224(2), 329-333 (1994) PMID: 7925345
プロフィール/メンバー
教授
教授経歴
1992年 福井医科大学医学部医学科 卒業
1992年 福井医科大学医学部 助手(第二生化学講座)
1994年 米国Yale大学医学部 客員助教授(免疫部門)
1995年 神戸大学医学部 助手(生化学第一講座)
2000年 神戸大学医学部 助教授
2001年 神戸大学大学院医学系研究科助教授(ゲノム科学講座)
2002年 科学技術振興事業団戦略的創造研究推進事業さきがけ研究21 研究員「認識と形成」
2005年 東京薬科大学生命科学部 教授(分子生化学研究室)
2020年 東京薬科大学 名誉教授
2020年より現職
1997年 博士(医学)神戸大学
2004年 日本生化学会 奨励賞 受賞
助教
助教経歴
2017年 東京薬科大学生命科学部 卒業
2022年 東京薬科大学大学院 生命科学研究科 修了
2020年より現職
2022年 博士(生命科学)東京薬科大学
研究員
稲留 涼子 (Ryoko Inatome)
博士(医学)神戸大学
伊藤 直樹 (Naoki Ito)
博士(生命科学)東京薬科大学
大学院生
- B4 池上 史悠 (Shiyuu Ikegami)
- B4 今井 一希 (Kauki Imai)
- B4 関根 志の (Shino Sekine)
- B4 武田 杏樹 (Anju Takeda)
- B4 眞鍋 大輝 (Taiki Manabe)
- B4 藪 陽登 (Haruto Yabu)
- B4 米沢 聖怜 (Seren Yonezawa)
D3 石川 悠人 (Yuto Ishikawa)
D3 大塩 聖 (Hijiri Oshio)
D2 田名部 大士 (Daishi Tanabu)
M2 鈴木 結衣子 (Yuiko Suzuki)
M2 廣瀬 駿 (Shun Hirose)
M2 松本 宗一郎 (Souichirou Matsumoto)
M2 美和 ゆかり (Yukari Miwa)
M1 江森 美咲 (Misaki Emori)
M1 岡田 直純 (Naozumi Okada)
M1 金谷 琴音 (Kotono Kanaya)
学部生

連絡先
住所
〒171-8588
東京都豊島区目白1−5−1
学習院大学 理学部 生命科学科
分子生化学(柳研究室)




