研究テーマ
カイコの変異体を用いた形質発現の分子機構解明
日本では、カイコ(Bombyx mori;カイコガ科)の変異系統が500以上も保存されています。分子生物学のモデル生物であるキイロショウジョウバエを除けば、これほど多くの変異系統を保持する昆虫種は他にありません。変異系統が示す特異な形質は、脱皮・変態や食性などの生理的形質から、産卵や営繭などの行動形質まで多岐にわたります。ショウジョウバエと異なり、幼虫期の斑紋や形態の変異が多いという特徴がありますが、卵・蛹(繭)・成虫で観察される変異形質も多くあります。

2008年にカイコゲノムが解読されて以降、世界の研究者たちが変異形質の原因遺伝子の探索に注力してきたにも関わらず、大部分の変異形質については未だに原因遺伝子が特定されていません。私たちの研究室では、次世代シーケンサーを活用し、これまで原因遺伝子の特定が難しいと考えられてきた変異形質の研究をおこなっています。現在は、営繭行動や産卵行動など、行動に関する変異体の解析を進めています。
エリサン(ヤママユガ科)の遺伝学
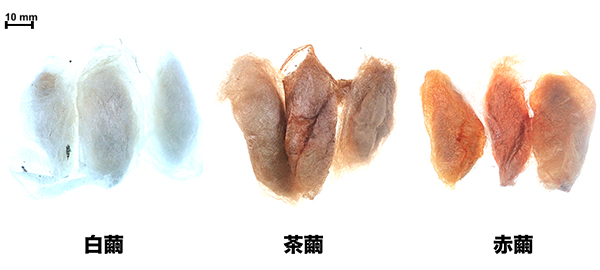
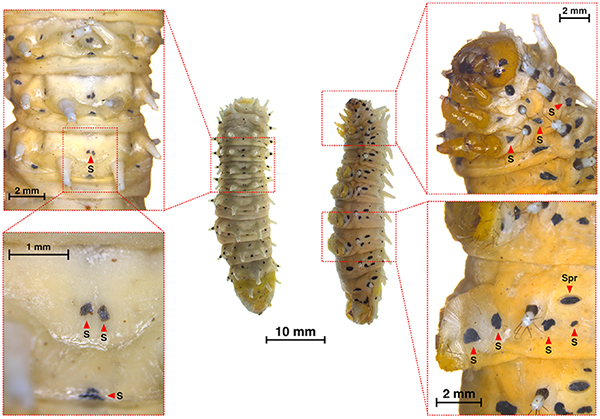
ヤママユガ科蛾類は、蛹での休眠性、青色-緑色系の鮮やかな幼虫体色、種ごとに異なる多様な食性など、カイコでは見られない様々な特性を持っています。当研究室の重要な研究対象であるエリサンSamia riciniは、同科に属する大型の蛾です。エリサンは、カイコと同様に家畜化された昆虫であり、野外には存在しません。多くのヤママユガ科蛾類は、幼虫の飼育が難しく、かつ飼育環境下における採卵も困難ですが、エリサンは、実験室内で容易に飼育することができ、継代も比較的簡単です。また、野生種であるシンジュサンSamia cynthia pryeriと交配して雑種を作ることもできます。私たちは、エリサンをはじめとするヤママユガ科蛾類の形質遺伝学を通して、カイコには存在しない諸形質の遺伝子基盤の解明に取り組んでいます。


鱗翅目昆虫のゲノム進化
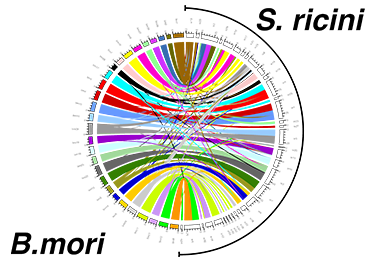
私たちの研究室の研究テーマに共通する目標は、「鱗翅目昆虫の進化の謎を遺伝子で紐解く」というものです。なにゆえこの昆虫はこのような生態を有するのか?という疑問に対して、近縁種との比較を通して、進化のトリガーとなった遺伝子を同定し、その機能を解明することで答えようとしています。そのために、鱗翅目昆虫のゲノムを種間・系統間で比較する必要があります。私たちは、バイオインフォマティクス技術を駆使し、鱗翅目昆虫の比較ゲノム解析をおこない、対象となる種や系統が「なぜ」「どのように」進化してきたのかを、ゲノムレベルで解明することに取り組んでいます。
ヤママユガ科・カイコガ科蛾類のゲノム編集技術の開発
2013年にCRISPR/Cas9が登場して以降、分子生物学において、遺伝子ノックアウトによる機能証明はほとんど必須のプロセスとなりました。とくに、鱗翅目昆虫においては、RNAiなどによる遺伝子発現の抑制(ノックダウン)が難しいので、遺伝子機能解析のためには必ず遺伝子をノックアウトする必要があります。
鱗翅目昆虫では、初めてカイコにおけるCRISPR/Cas9による遺伝子ノックアウトが有効であることが報告され、その後コナガなどでも同法によるノックアウトが可能であることが報告されています。しかし、非モデル生物種において新しく遺伝子ノックアウト系を確立することは、依然として骨の折れる作業であり、カイコの近縁種でも簡単ではありません。私たちの研究室では、エリサンおよび他のヤママユガ科・カイコガ科蛾類を対象に、CRISPR/Cas9やTALENによる遺伝子ノックアウト法を開発しています。合わせて、遺伝子ノックアウトに代わる機能解析技術の開発や遺伝子ノックイン技術の開発にも取り組んでいます。
活動実績
最近の論文発表
(2019年4月から現在までに発表した論文を発表年月日の新しい順に掲載)Fujii T, Hino M, Fujimoto T, Kakino K, Kaneko Y, Abe H, Lee JM, Kusakabe T, Shimada T. (2025) Peroxiredoxin 6 is essential for the posttranslational activation of xanthine dehydrogenase in the uric acid synthesis of Bombyx mori. Insect Biochemistry and Molecular Biology 29: 104264. 論文を見る
Lee J, Fujimoto T, Sahara K, Toyoda A, Shimada T. (2025) Comprehensive genome annotation of Bombyx mori p50ma strain, a newly developed standard strain. Scientific Data 12(1): 359. 研究成果・プレスリリース 論文を見る
Lee J, Fujimoto T, Yamaguchi K, Shigenobu S, Sahara K, Shimada T. (2025) Comprehensive genome annotation of Trilocha varians, a new model species of Lepidopteran insects. Scientific Data 12(1): 124. 研究成果・プレスリリース 論文を見る
Lee J, Kiuchi T, Yamaguchi K, Shigenobu S, Toyoda A, Shimada T. (2025) A chromosome-level genome assembly of wild silkmoth, Bombyx mandarina. Scientific Data 12(1): 27. 研究成果・プレスリリース 論文を見る
Fujii T, Kuwazaki S, Abe H, Fujimoto T, Hino M, Yamamoto K, Shimada T. (2024) Genetic analysis of the two fused chromosomes derived from the sex-limited strain TWPB of the silkworm, Bombyx mori. Journal of Insect Biotechnology and Sericology 93(3): 23-34. 論文を見る
Lee J, Fujimoto T, Yamaguchi K, Shigenobu S, Sahara K, Toyoda A, Shimada T. (2024) W chromosome sequences of two bombycid moths provide an insight into the origin of Fem. Molecular Ecology 33(14): e17434. 研究成果・プレスリリース 論文を見る Wiley社の"Top cited article 2025"に選ばれました(Certificate)(2024年1月〜12月にMolecular Ecology誌に掲載された論文のうち被引用数が上位10%である論文が選ばれる)
Tomihara K, Tanaka S, Katsuma S, Shimada T, Kobayashi J, Kiuchi T. (2023) Recessive embryonic lethal mutations uncovered in heterozygous condition in silkworm semiconsomic strains. Insect Biochemistry and Molecular Biology 155: 103933. 論文を見る
Fujii T, Kubo M, Kuwazaki S, Yamamoto K, Ohnuma A, Banno Y, Shimada T. (2022) DNA sequence analysis of a chromosomal aberration in irradiation induced burnt (Bu) mutant of Bombyx mori. Journal of Insect Biotechnology and Sericology 91: 41-50. 論文を見る
Fujii T, Kiuchi T, Daimon T, lto K, Katsuma S, Shimada T, Yamamoto K, Banno Y. (2021) Development of interspecific semiconsomic strains between the domesticated silkworm, Bombyx mori and the wild silkworm, B. mandarina. Journal of Insect Biotechnology and Sericology 90: 33-40. 論文を見る
Dai X, Kiuchi T, Zhou Y, Jia S, Xu Y, Katsuma S, Shimada T, Wang H. (2021) Horizontal gene transfer and gene duplication of β-fructofuranosidase confer lepidopteran insects metabolic benefits. Molecular Biology and Evolution 38: 2897-2914. 論文を見る
Lee J, Nishiyama T, Shigenobu S, Yamaguchi K, Suzuki Y, Shimada T, Katsuma S, Kiuchi T. (2020) The genome sequence of Samia ricini, a new model species of lepidopteran insect. Molecular Ecology Resources 21: 327-339. 論文を見る
Zhou Y, Li X, Katsuma S, Xu Y, Shi L, Shimada T, Wang H. (2019) Duplication and diversification of trehalase confers evolutionary advantages on lepidopteran insects.
Molecular Ecology 28: 5282-5298. 論文を見る
Tomihara K, Satta K, Shimada T, Kiuchi T. (2019) CRISPR/Cas9-mediated somatic mutation of the sex-linked translucent (os) gene in the silkworm, Bombyx mori. Journal of Insect Biotechnology and Sericology 88: 31-38. 論文を見る
Kawamoto M, Jouraku A, Toyoda A, Yokoi K, Minakuchi Y, Katsuma S, Fujiyama A, Kiuchi T, Yamamoto K, Shimada T. (2019) High-quality genome assembly of the silkworm, Bombyx mori. Insect Biochemistry and Molecular Biology 107: 53-62. 論文を見る
プロフィール/メンバー
教授
教授経歴
1982年 東京大学農学部 卒業
1984年 東京大学大学院農学系研究科 修士課程 修了
1987年 東京大学大学院農学系研究科 博士課程 修了
1987年 財団法人がん研究振興財団 リサーチ・レジデント
1988年 日本学術振興会 特別研究員(PD)
1988年 国立予防衛生研究所(現 国立感染症研究所)研究員
1990年 東京大学農学部 助手
1995年 東京大学農学部 助教授
1996年 東京大学大学院農学生命科学研究科 助教授
2004年 東京大学大学院農学生命科学研究科 教授
2020年 東京大学 名誉教授
2019年より現職(学習院大学理学部 教授)
嶋田教授のウェブページ
助教
高井嘉樹 (Hiroki Takai)
研究員
客員研究員
・李允求(信州大学 テニュアトラック助教)[2026年1月1日〜]
科研費研究員
・1名
現在在籍している学生
(2026年度)
大学院生
・博士後期課程
・D3〜D1: 0名
・博士前期課程
・M2: 0名
・M1: 1名
学部学生
・4年生: 6名
過去に在籍した学生
大学院生(博士前期課程)の在籍
・2025年度 M2: 3名 M1: 0名
・2024年度 M2: 0名 M1: 3名
・2023年度 M2: 1名 M1: 0名
・2022年度 M2: 1名 M1: 1名
・2021年度 M2: 0名 M1: 1名
・2020年度 M2: 0名 M1: 0名
・2019年度 M2: 0名 M1: 0名
4年生の在籍
・2025年度 6名
・2024年度 6名
・2023年度 4名(外研1名を含む)
・2022年度 8名(外研1名を含む)
・2021年度 4名
・2020年度 5名
・2019年度 6名



