リリース
-

2026.05.22
リリース
研究成果
知識モデルにおけるunawareness表現の不可能性定理に関する新解釈を提示
-
2026.05.05
共同プレスリリース
研究成果
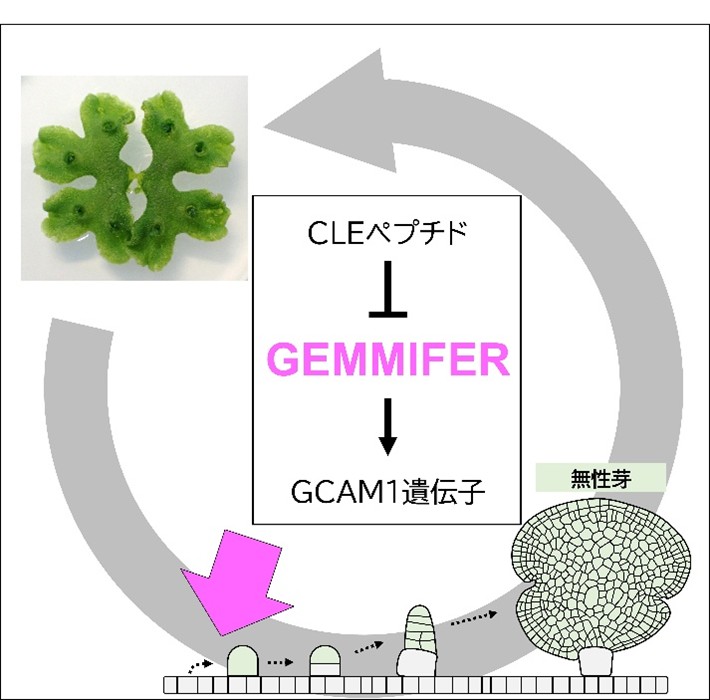
ゼニゴケのクローン繁殖を誘導する遺伝子を発見―農作物種を含むさまざまな植物への応用に期待―
-
2026.04.24
共同プレスリリース
研究成果
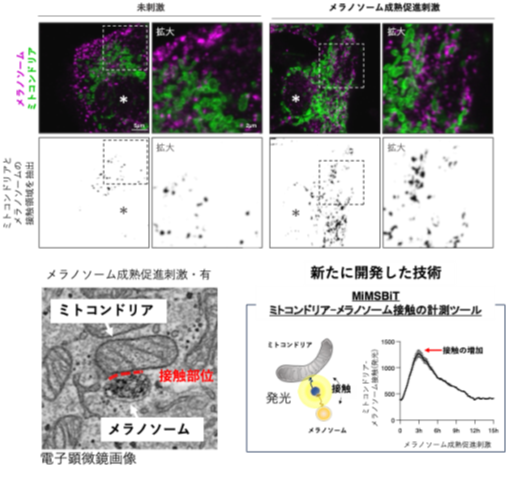
ミトコンドリアとメラノソームの接触がメラニン色素形成を制御―メラニン色素形成を支える細胞内機構を解明―
-

2026.04.22
共同プレスリリース
研究成果
老化で弱ったミトコンドリアを"増やして強くする"新規化合物を発見―加齢に伴う心機能低下を改善、栄養過多による寿命低下を抑制―
-
2026.04.07
研究成果
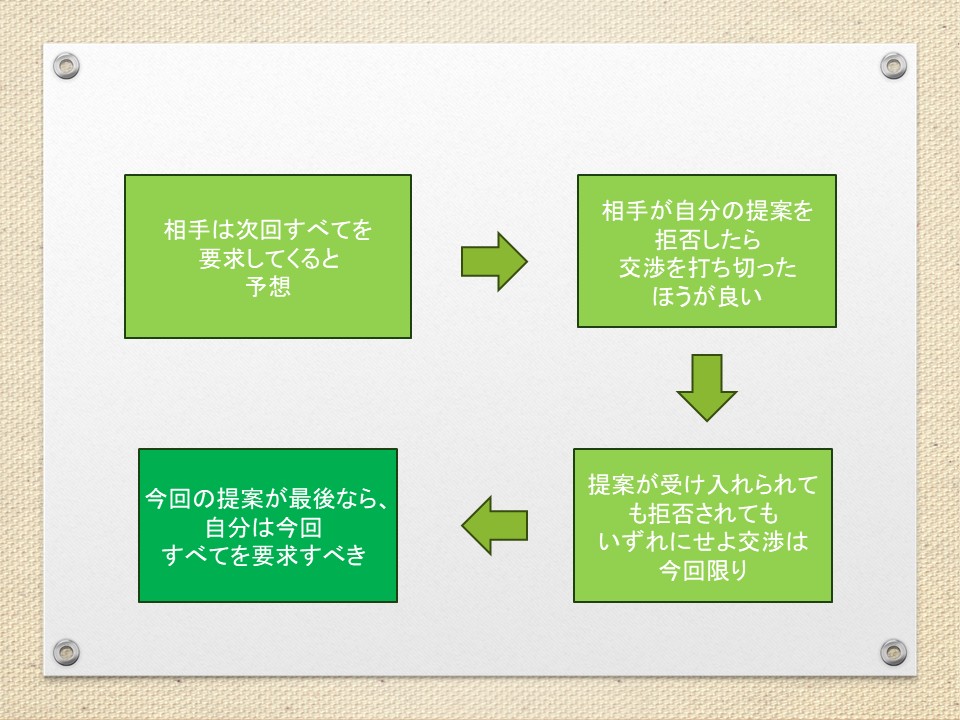
交渉において、提案を拒否したら打ち切るという脅し(最後通牒)が有効なのはどうしてか
-
2026.04.02
プレスリリース
研究成果
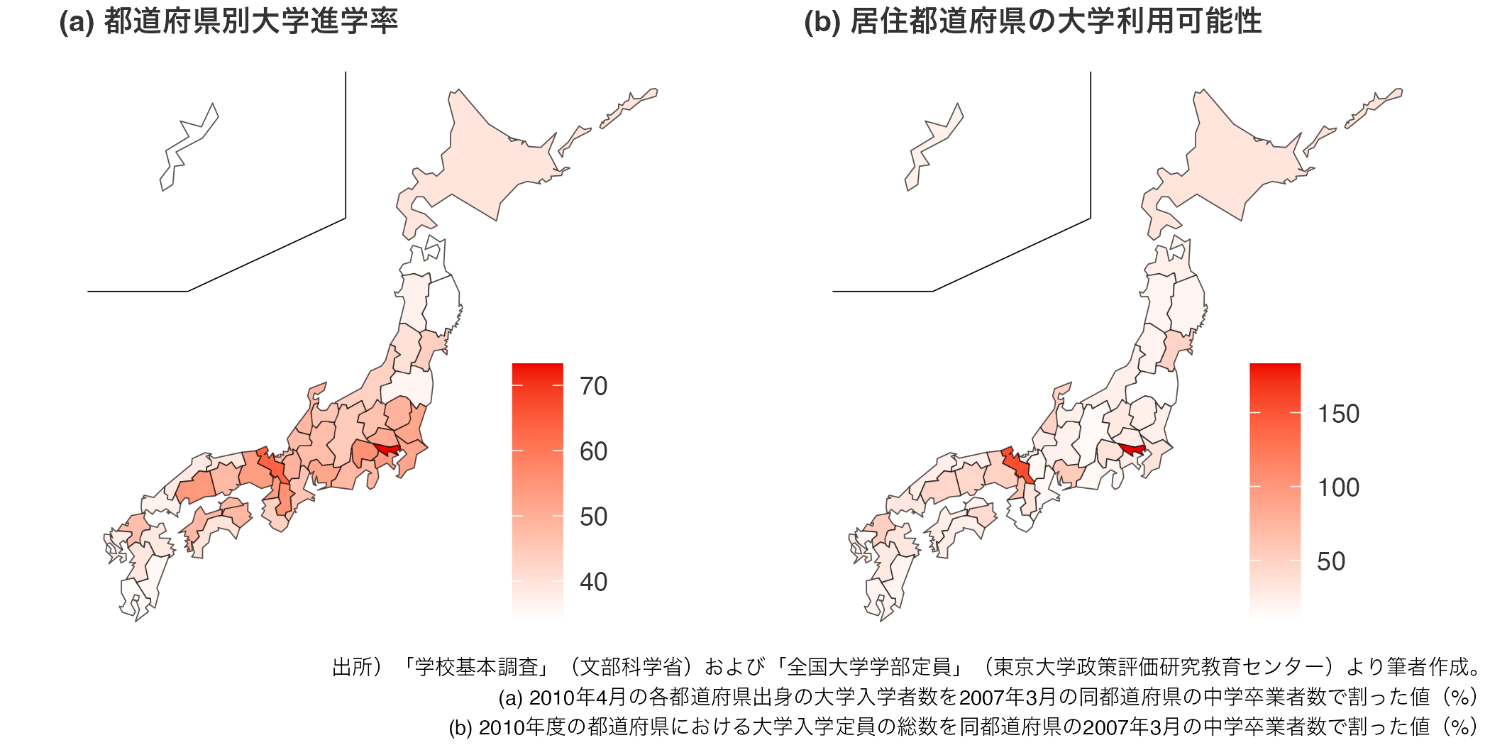
大学の偏在が進学率の地域間格差を拡大する 大学定員増加が地域の大学進学率に与える効果を実証
-

2026.03.24
プレスリリース
学習院大学発ベンチャー企業の株式会社マイトジェニックがミトコンドリア研究の新成分「マイトルビン」でダイドーグループと共同研究開始
-
2026.03.10
プレスリリース
研究成果
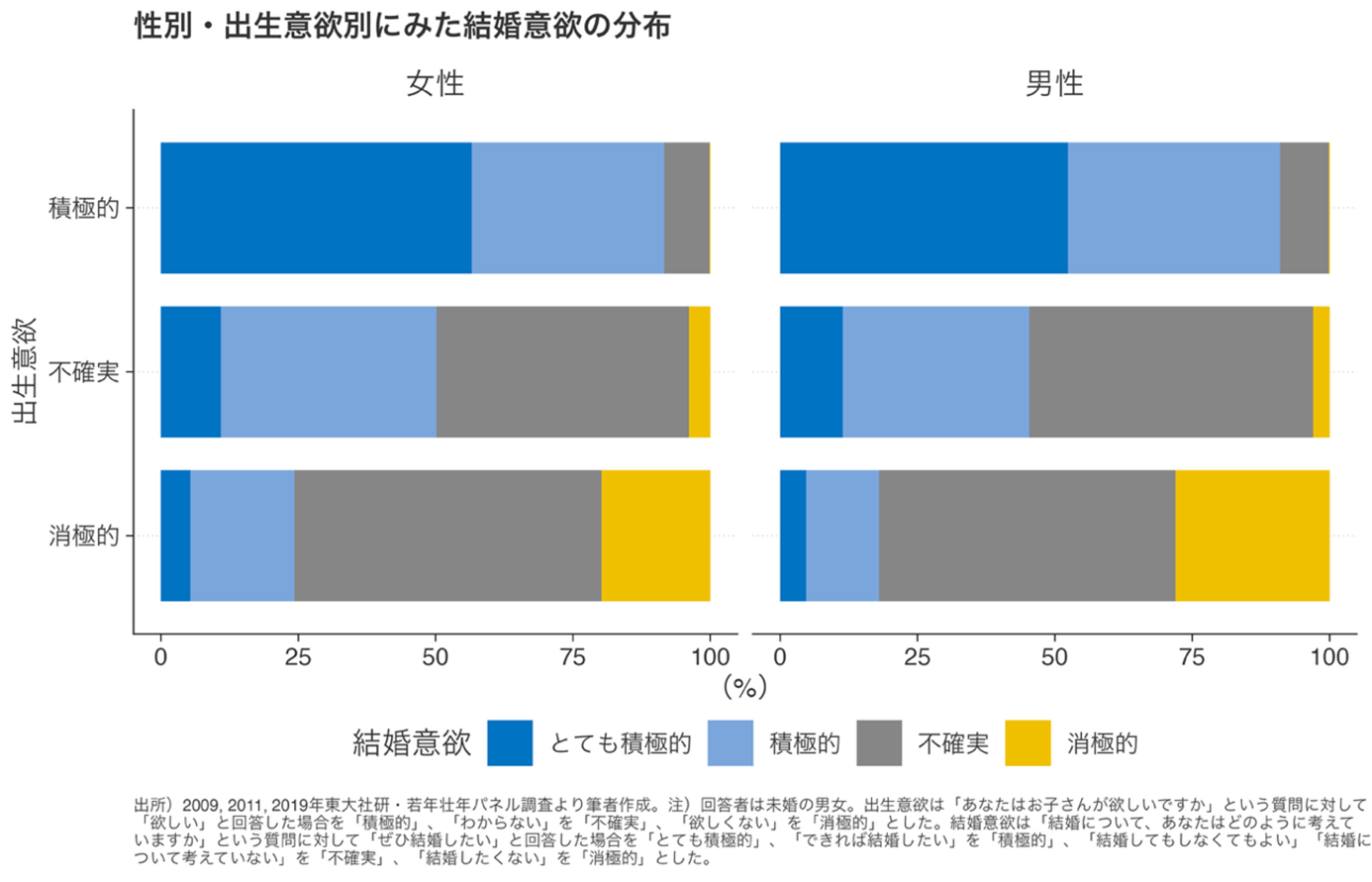
子どもを持ちたくない・迷っていることが結婚を遅らせる要因に 東アジアの少子化の原因への新たな示唆
-
2025.12.24
プレスリリース
研究成果
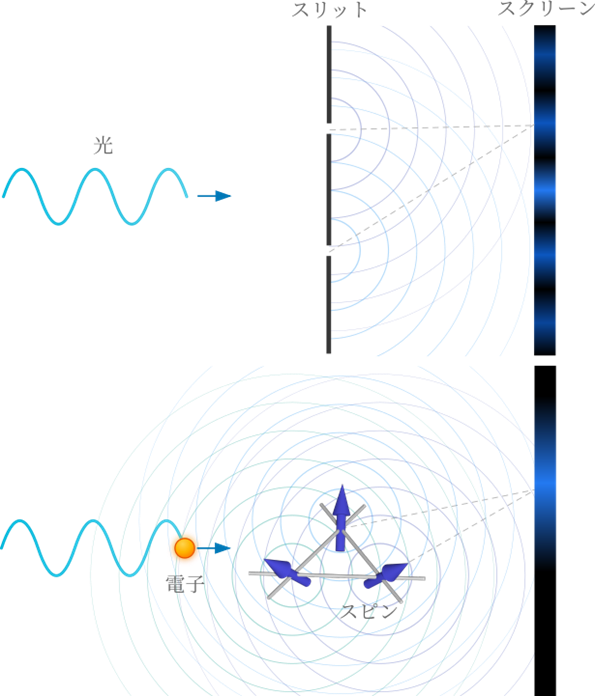
高伝導金属における異常ホール効果を理解する理論を提唱 -電子の量子位相干渉と磁気相関の協奏効果を理論的に解明-
-

2025.12.23
プレスリリース
学習院大学とキャンパスクリエイトの産学連携協定により実用化へ前進 -学習院大学・稲熊教授の研究成果、 中島産業がサブライセンスを取得-
-
2025.12.03
プレスリリース
研究成果
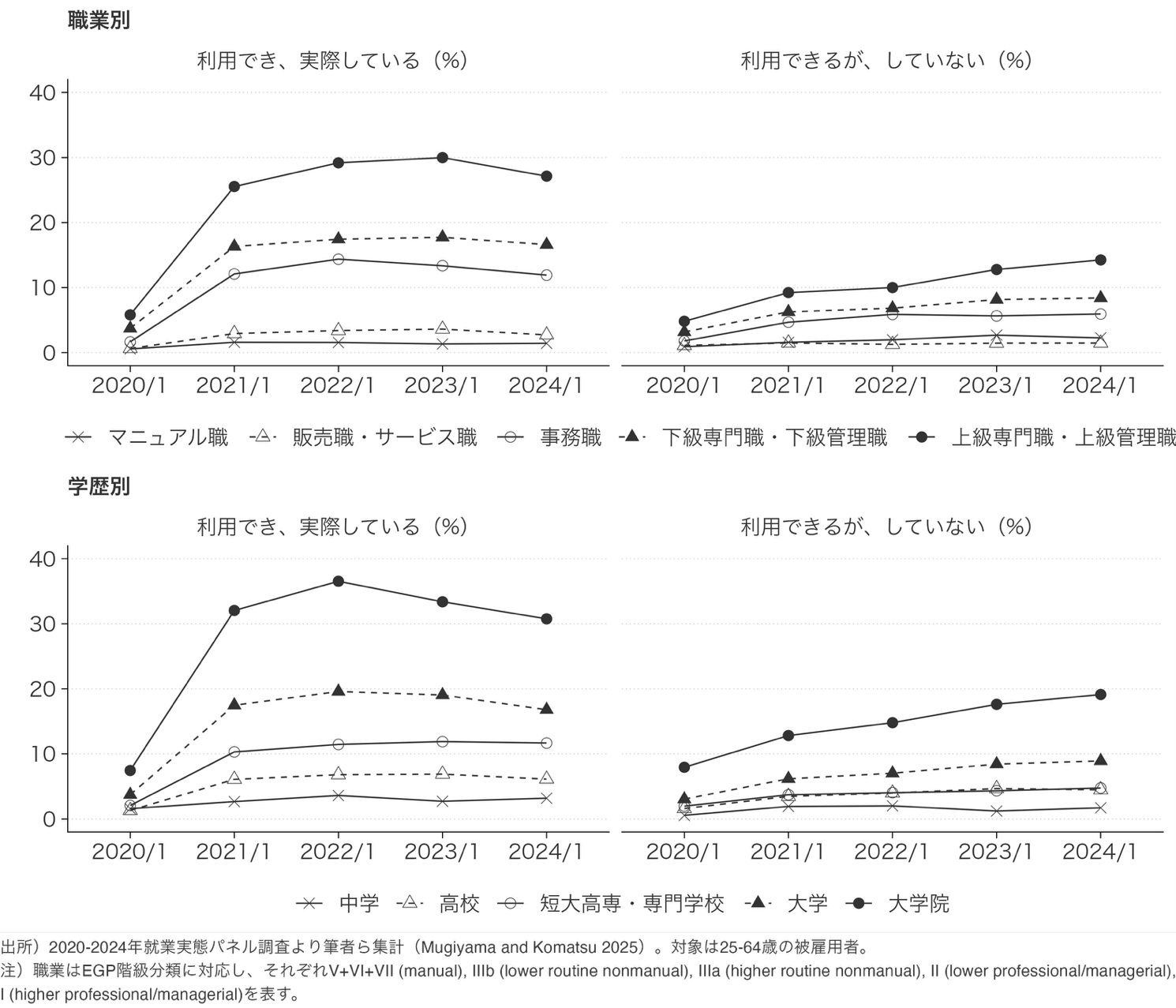
コロナ禍で広がったテレワークの「選択肢」の格差 2020-2024年の継続調査を用いて制度の普及率が職業と学歴によって異なることを実証
-

2025.10.20
研究成果
進化の頂点or袋小路?:ミズギワカメムシのオス附属腺




