アルツハイマー病の発症前に脳の異常を検出する新たな方法を開発―VRゴーグルを用いて身体に負担を与えず、低コストで実施可能―
2024.02.12
共同プレスリリース
研究成果
アルツハイマー病の発症前に脳の異常を検出する新たな方法を開発
―VRゴーグルを用いて身体に負担を与えず、低コストで実施可能―
研究成果のポイント
- アルツハイマー病の根本治療薬の出現により認知機能検査に異常が出現する前のアルツハイマー病超早期の診断法開発が求められています。
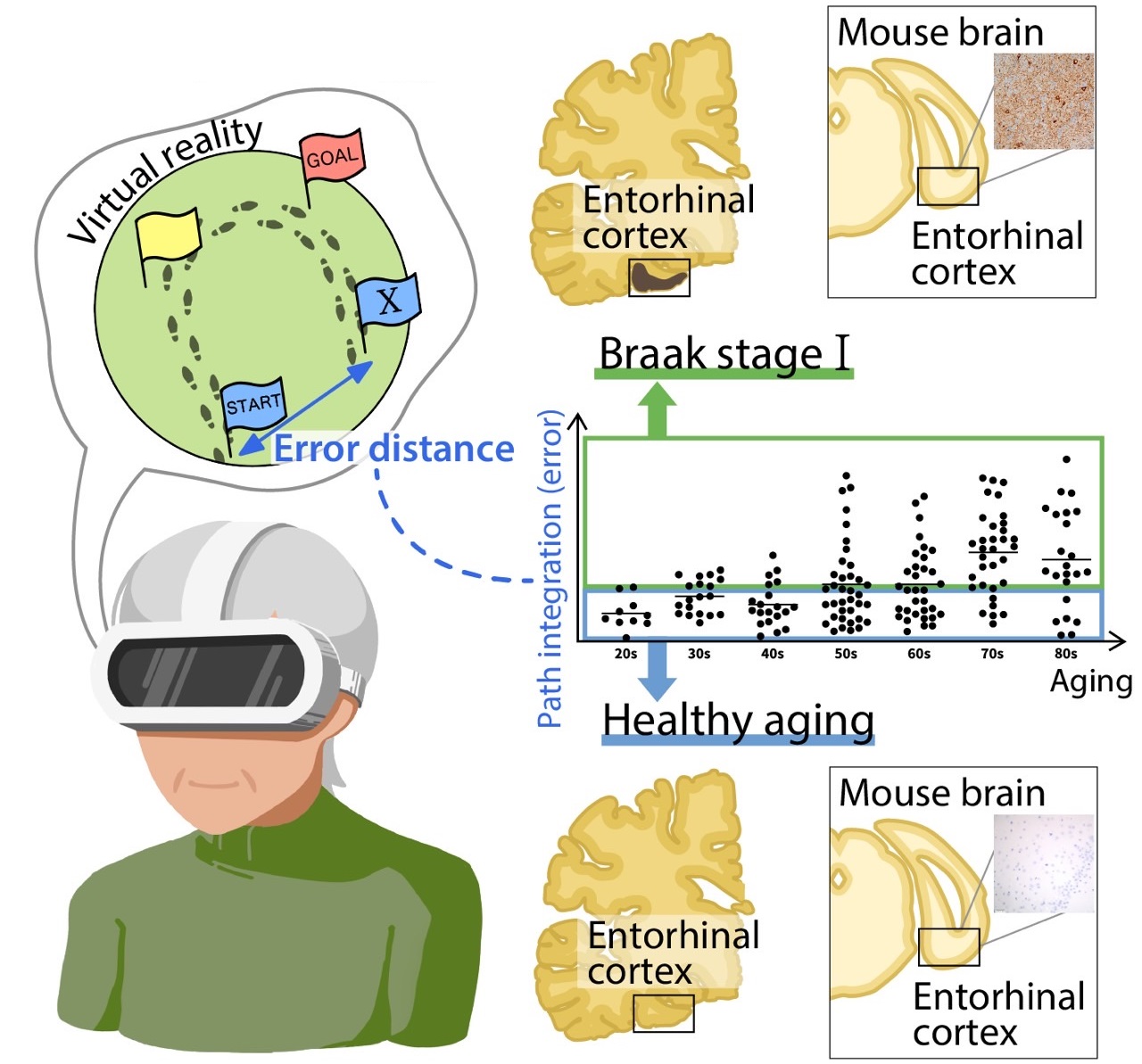
- 本研究では最初期病変が起こる嗅内野※1に注目し、その機能の一つであるグリッド細胞の活動をVRゴーグルを用いて経路統合能のエラー距離として測定する方法を開発し、エラー距離が20~90歳代の記憶に障害を持たない被験者の閾値を超える割合は剖検脳を用いた横断研究で報告された嗅内野病変を持つ人の割合と一致することを示しました。
- モデル動物を用いた実験で、嗅内野にリン酸化タウ蓄積を示すマウスでは空間記憶に障害を示さず、経路統合能低下が引き起こされることを確認しました。
- 今回開発したVRゴーグルを用いた方法で安価で簡便に脳の機能的スクリーニングを行うことが期待できます。さらに血液検査等で脳内の生化学的変化を加えることで精度良くアルツハイマー病発症に至る超早期の脳の状態を知ることが可能になると考えられます。このことは、治療のみならず、予防にも役立つ可能性があります。
概要
学習院大学大学院自然科学研究科の大学院生 小池力さん、添田義行助教、髙島明彦教授、藤田医科大学脳神経内科学の渡辺宏久教授、滋賀医科大学の石垣診祐教授、藤岡祐介助教、東京大学の内田和幸教授、チェンバーズ ジェームズ助教、大学院生 高市雄太さんからなる研究チームが、アルツハイマー病の発症前にVRゴーグルを用いて脳の異常を検出する新たな方法の開発に成功しました。
アルツハイマー病は早期に発見すれば、予防や治療の効果が高まる可能性があります。しかし現在の診断法では、症状が現れる前にアルツハイマー病を検出することは困難です。
今回、研究チームはVRゴーグルを用いて、脳の空間認知機能である経路統合能※2を測定する方法を開発しました。本研究では、VRゴーグルを用いたナビゲーション機能を測定することでアルツハイマー病に至る最初の病変である嗅内野の神経原線維変化※3を検出することに成功しました。この方法により安価で非侵襲的、簡便に脳の状態を知ることができ、ヒトにおけるアルツハイマー病の予防や治療に役立てることが期待されます。
研究の背景
アルツハイマー病は認知症の最も一般的な原因であり、世界中で数千万人の人々が苦しんでいます。しかし現在の診断法では、症状が現れる前にアルツハイマー病を検出することは困難です。早期に発見すれば、予防や治療の効果が高まる可能性がありますが、そのためには脳内で起こっている微細な変化を捉える必要があります。
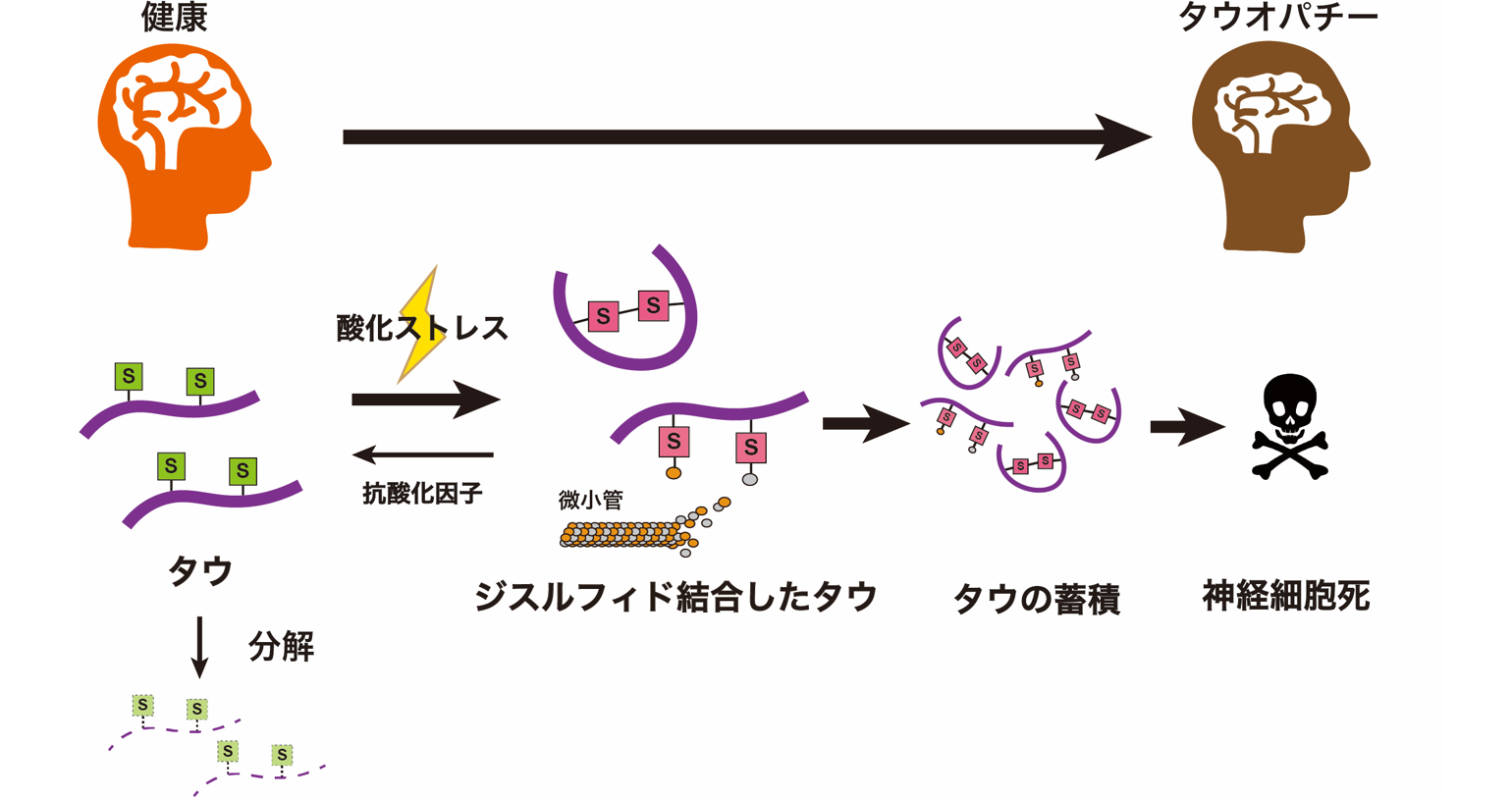
アルツハイマー病の脳ではβアミロイドの蓄積(老人斑)、リン酸化タウの細胞内蓄積(神経原線維変化)が観察されます。神経原線維変化は嗅内野から始まり大脳辺縁系、新皮質へと順番に広がり、脳機能を緩徐に低下させます。βアミロイドはこの神経原線維変化が嗅内野から広がる速度を加速することでアルツハイマー病を引き起こします。嗅内野の病変を知ることができれば予防や治療が可能となりますが、認知症診断に用いられるMMSEやCDRなどの認知機能検査では検出することはできません。
嗅内野は側頭葉内側部に位置し一次感覚野の情報を受容し、海馬、大脳基底核、前頭葉などと相互作用します。嗅内野にはグリッド細胞が存在し、この働きによって空間内の位置情報を得ています。空間のある地点から他の地点へ移動する(ナビゲーション)時、嗅内野を中心として海馬、前頭葉などナビゲーション関連部位の活性化が起こります。これらの部位はアルツハイマー病の病変の一つである神経原線維変化の好発部位になります。このことから、アルツハイマー病では初期からナビゲーション障害が顕在化することが知られています。
研究の内容
今回、アルツハイマー病の認知症発症に関係すると考えられているタンパク質「リン酸化タウ」の嗅内野における蓄積と、脳の空間認知機能「経路統合能」の低下との関係を調べました。経路統合能とは、自分の移動した距離や方向を記憶し、出発地点や目的地点へ戻る能力のことです。この能力は、脳の側頭葉内側にある「嗅内野」という部位が担っています。
研究チームは、VRゴーグルを用いて経路統合能を測定する方法を開発しました。被験者は、VRゴーグルで見える仮想空間で三角形の経路を歩き、その後にスタート地点へ戻るように指示されます。このとき、被験者が歩いた距離や方向を正確に判断できるかどうかを評価しました。
その結果、経路統合能が低下している各年齢群の被験者の割合が嗅内野に神経原線維変化が出現している人の割合と一致することが分かりました。さらに、マウスモデルを用いた研究ではリン酸化タウが嗅内野に蓄積したマウスでは、経路統合能が低下することが示され、嗅内野における神経原線維変化と経路統合能低下の関係を確認しました。経路統合能の異常は、アルツハイマー病の最初の兆候であると考えられます。
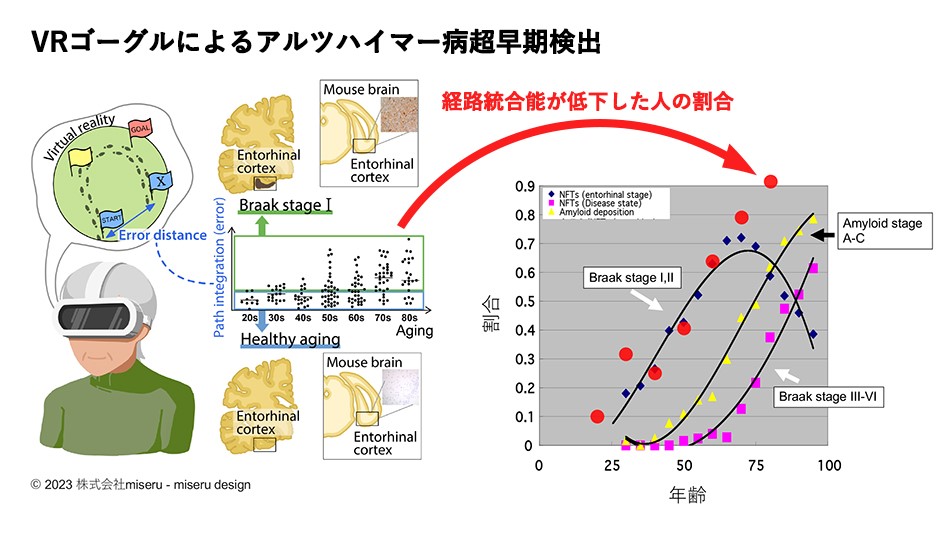
嗅内野に神経原線維変化が起こると経路統合能の低下が起こる。
本研究成果が社会に与える影響(本研究成果の意義)
本研究成果は、アルツハイマー病の発症前に脳の異常を検出する新たな方法を提供します。VRゴーグルを用いた経路統合能の測定は、簡便で非侵襲的、低コストで行えるため、広く普及することが可能です。
アルツハイマー病治療薬としてβアミロイドを除去するレカネマブが承認されています。今回開発したVRゴーグルを用いた方法で脳の機能的スクリーニングを行い、血液検査等で脳内の生化学的変化を捉えることでさらに精度良くアルツハイマー病発症に至る超早期の脳の状態を知ることが可能となります。経路統合能が低下した方にアミロイドPET検査、または脳脊髄液検査でβアミロイド蓄積の有無を調べることによって、アルツハイマー病治療までのプロセスの効率化に寄与すると考えられます。経路統合能が低下しているけれどもβアミロイドが陰性の方は生活習慣の改善などでアルツハイマー病の予防が可能になります。今後この技術をさらに改良し、通常の生活行動からアルツハイマー病の予兆を見出し、アルツハイマー病の予防や治療にさらに役立てることを目指しています。
特記事項
本研究成果は2024年2月12日(日本時間9時1分)に国際学術誌Brain. Communicationのオンライン版に掲載されます。本研究は、AMEDの課題番号JP15km0908001、JSPSの新学術"Singularity Biology (No. 8007)" (18H05414)の支援を受けて行われました。また、本発表は学習院大学グランドデザイン 2039「国際学術誌論文掲載補助事業」より掲載費の助成を受けています。
【論文情報】
雑誌:Brain. Communication
著者名:Riki Koike, Yoshiyuki Soeda, Atsushi Kasai, Yusuke Fujioka, Shinsuke Ishigaki, Akihiro Yamanaka, Yuta Takaichi, James K. Chambers, Kazuyuki Uchida, Hirohisa Watanabe, Akihiko Takashima
DOI:10.1093/braincomms/fcad359
用語説明
※1 嗅内野
脳の側頭葉内側にあり、視覚、聴覚、体性感覚を受容し、それらの情報を統合し海馬や大脳皮質へ送っています。嗅内野にはグリッド細胞と呼ばれる空間ナビゲーションに関係する細胞が存在しています。加齢すると嗅内野にアルツハイマー病の病理学的特徴の一つである神経原線維変化が最初に形成される場所です。この後、神経原線維変化が大脳辺縁系、大脳新皮質へ広がると認知症を引き起こします。
※2 経路統合能
経路統合能とは、自分の移動した距離や方向を記憶し、出発地点や目的地点へ戻る能力のことです。この能力は、脳の側頭葉内側にある「嗅内野」という部位が担っています。
※3 神経原線維変化
アルツハイマー病の病理変化の一つで神経細胞内にリン酸化タウが凝集した状態です。細胞内でこのような変化が起こるとその領域では数倍の神経細胞死が起こっています。そのため、神経原線維変化が脳内で広がることによって認知症を引き起こします。